Антисептические средства: возможности использования при респираторных инфекциях в условиях пандемии COVID-19
2021.03.16Г.Х.Викулов
Российский университет дружбы народов (РУДН), Москва, Российская Федерация; Научный информационный центр по профилактике и лечению вирусных инфекций, Москва, Российская Федерация; Герпетический центр, клиника Доктор.Prof, Москва, Российская Федерация
В статье изложены актуальные аспекты применения антисептиков при респираторных инфекциях, представлен обзор и рекомендации по применению гипохлорита натрия у пациентов с ОРВИ, гриппом. Проведен анализ возможностей применения антисептиков для профилактики COVID-19.
Ключевые слова: инфекционные болезни, ОРВИ, антисептики, санитайзеры, COVID-19, профилактика респираторных инфекций, гипохлорит натрия
Для цитирования: Викулов Г.Х. Антисептические средства: возможности использования при респираторных инфекциях в условиях пандемии COVID-19. Инфекционные болезни. 2020; 18(2): 58–66. DOI: 10.20953/1729-9225-2020-2-58-66
Острые респираторные инфекции (ОРИ) – это заболевания полиэтиологичной природы. В настоящее время известно более 300 возбудителей ОРИ, среди которых преобладают вирусы, вызывающие развитие острых респираторных вирусных инфекций (ОРВИ). Преимущественное как эпидемиологическое, так и клиническое значение имеют риновирусы (30–50%), вирусы гриппа А и В (5–15%), герпесвирусы человека, новые и возвращающиеся возбудители инфекций (например, вирусы кори, коронавирусы, возбудитель коклюша, бокавирусы, метапневмовирусы и др.), обусловливающие высокую вспышечную заболеваемость с преобладанием в северном полушарии в осенне-зимний период; значительно реже ОРИ вызывают аденовирусы, вирусы парагриппа, респираторно-синцитиальный вирус, другие патогены вирусной, бактериальной, грибковой природы и также практически у каждого второго пациента встречаются смешанные инфекции.
Профилактика ОРВИ и гриппа предусматривает применение:
1) ограниченного спектра противовирусных препаратов,
2) сезонной иммунопрофилактики перед началом ежегодной эпидемии гриппа,
3) препаратов этиотропной терапии,
4) иммуномодулирующих препаратов в сочетании с этиотропной терапией (по показаниям).
Общим недостатком этиотропной терапии ОРВИ и гриппа является ограниченный перечень эффективных препаратов, узкий спектр их действия (озельтамивир, занамивир, ремантадин), серьезные побочные эффекты (например, рибавирина, ремантадина, озельтамивира, препаратов системных интерферонов), не все препараты имеют высокий профиль безопасности у детей (например, тилорон). Возможности иммунопрофилактики ограничены как узким спектром инфекций (грипп, пневмококковая инфекция, коклюш, корь, ветряная оспа, гемофильная инфекция, дифтерия, RS-инфекция, туберкулез, менингококковая инфекция), так и в связи с осознанным отказом и недоверием к вакцинации, включенным ВОЗ в опубликованный ежегодный список десяти глобальных угроз человечеству. Для всех противогриппозных вакцин обязательным является соответствие циркулирующих актуальных штаммов тем, которые входят в состав обновленных вакцин. Несоответствие штаммового состава приводит к частичной и недостаточной эффективности вакцинации [1–4].
Коронавирусная инфекция
Коронавирусы являются самой большой группой из известных РНК-содержащих респираторных вирусов, которые регистрируются с 1965 г. В структуре ОРВИ доля коронавирусных инфекций варьирует от 5 до 28%. До 2002 г. коронавирусы вызывали легкие ОРВИ в 5–7 раз чаще у детей, чему взрослых. С 2002 г. коронавирусы являются причиной эпидемических вспышек серьезных по тяжести респираторных заболеваний: SARS-инфекции, или тяжелого острого респираторного синдрома, с 2012 г. описана MERS-инфекция, или ближневосточный респираторный синдром. В декабре 2019 г. в Китае был выявлен новый тип коронавируса, который преодолел межвидовой барьер и стал передаваться от животных человеку, а затем аэрогенно воздушно-капельным и воздушно-пылевым путем и контактным механизмом от человека к человеку (обсуждается также фекально-оральный путь передачи), вызвавший вспышку новой коронавирусной пневмонии. 11 февраля 2020 г. ВОЗ присвоила название новой коронавирусной инфекции, вызванной вирусом SARSCoV-2, – COVID-19, пандемия которой продолжается по настоящее время с вовлечением населения из более 200 государств. По состоянию на 19.06.2020 число инфицированных SARS-CoV-2 в мире составило 8 501 444 человека, погибших – 454 230 человек, текущая летальность варьирует от 0,06% в Сингапуре до 14,49% в Италии [5]. Согласно анализу клинического состояния 1099 пациентов на 28 февраля 2020 г., у 91,1% больных COVID-19 была диагностирована полисегментарная пневмония [6].
Ежегодно в России выявляют от 700 тыс. до 2 млн внегоспитальных пневмоний, до 30–35% случаев связаны с вирусами гриппа и другими патогенами. В 2020 г. существенно увеличилась доля коронавирусных внегоспитальных пневмоний – до 20–25% [6–10]. Развитие пандемии COVID-19 свидетельствует о том, что SARS-CoV-2-инфекция является угрозой для мирового здравоохранения, что простимулировало введение беспрецедентных карантинных мероприятий, создание тест-систем для молекулярно-биологической и серологической диагностики, проведение тщательного непрерывного эпидемиологического мониторинга, а также интенсификацию разработок клинических исследований этиотропных противовирусных препаратов и эффективных мер профилактики, включая иммунопрофилактику [11–16].
Использование антисептиков в качестве средств индивидуальной защиты
Основными входными воротами для SARS-CoV-2 являются полость носа и ротовая полость. Исследования показывают, что вирусная нагрузка наиболее высока в носоглотке и в слюне, попадание и распространение возбудителя в нижние дыхательные пути может осуществляться постепенно как из верхних дыхательных путей, так и путем быстрой ингаляции возбудителя, что является основой заболеваний и причиной прогрессирования поражения легочной ткани, особенно у пациентов из групп риска [17].
SARS-CoV-2 присутствует в слюне инфицированных лиц до 3 недель. Кроме того, было подтверждено, что возбудитель проникает в клетки тем же путем, что и SARS-CoV, то есть через клеточный рецептор ACE225, а также через еще один рецептор – CD147+. Было продемонстрировано, что АСЕ2+ эпителиальных клеток протоков слюнных желез являются классом ранних мишеней инфекции как для SARSCoV, так и для SARS-CoV-2. Эти данные обосновывают применение антисептиков местно в полости рта и носовой полости [18–20].
В России были изданы временные методические рекомендации по COVID-19 [21], но в них недостаточно подробно описаны рекомендации по применению антисептиков и средств дезинфекции.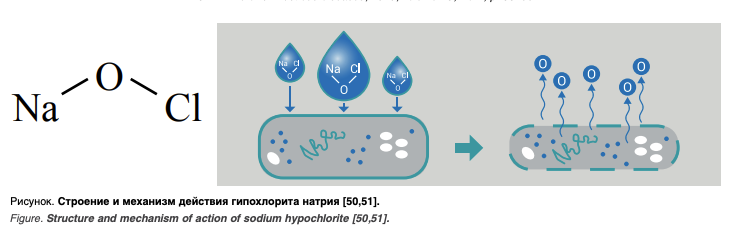
Одним из главных направлений в деятельности медицинских организаций является обеспечение безопасности пациентов и персонала. Наиболее существенной составляющей всего комплекса безопасности считается профилактика инфекций, связанных с оказанием медицинской помощи. Деятельность медицинских организаций на современном уровне характеризуется широким внедрением в практику новых методов терапии и диагностики, что ведет к внедрению новых технологий и медицинских изделий, в том числе инструментов, медицинской техники, новых материалов. Важнейшим аспектом неспецифической профилактики госпитальных инфекций является использование химических средств дезинфекции и стерилизации. В условиях интенсивного внедрения и использования современных медицинских технологий, с одной стороны, и большого разнообразия антисептиков и дезинфекционных средств, с дру-гой стороны, перед медицинскими организациями стоит сложная задача оптимального выбора эффективных и безопасных химических средств дезинфекции и стерилизации. Главными требованиями, предъявляемыми к современным дезинфицирующим средствам, применяемым в медицинских организациях, являются их эффективность и безопасность [22].
Главная цель при использовании средств индивидуальной защиты, к которым относятся антисептики, – это повышение эффективности профилактики ОРВИ, выражающееся в предупреждении заболевания в период эпидемий, уменьшение тяжести течения заболевания, снижение количества осложнений у заболевших, обеспечиваемое вирулицидным действием средств с доказанной эффективностью, способностью антисептиков не подавлять естественную микробиоту и местный иммунитет слизистых оболочек, способностью активировать окислительные процессы в тканях [23].
Выбор антисептиков, действующих на SARS-CoV-2
В связи с появлением пандемических штаммов вирусов, включая вирусы гриппа А, SARS-CoV-2 (2019-nCoV), ростом антибиотикорезистентности, широким применением антисептиков в медицинских учреждениях (профилактика инфекций, связанных с оказанием медицинской помощи), необходимостью экстренной и плановой профилактики инфекций во время путешествий и после контакта с пациентами, имеющими клинические проявления ОРВИ, гриппа или подтвержденные случаи COVID-19, не теряет актуальности выбор наиболее эффективных и безопасных антисептических средств с целью ежегодной профилактики респираторных инфекций для групп риска [24].
В настоящее время имеются сотни зарегистрированных в установленном порядке дезинфицирующих и антисептических средств из разных групп химических соединений и различающихся по составу рецептур. На основании химической классификации средств для дезинфекции выделяют средства, выделяющие кислород [22].
Особое внимание в качестве средства индивидуальной защиты при респираторных инфекциях среди антисептиков привлекает гипохлорит натрия в концентрации от 0,05% до 0,1% (рисунок). Гипохлорит натрия входит в список дезинфицирующих средств, которые были квалифицированы для использования против SARS-CoV-2 Агентством по охране окружающей среды США.
В связи с тем, что выявлены сопоставимые генетические характеристики SARS-CoV и MERS-CoV, предполагается, что SARS-CoV-2, вероятно, может быть чувствительным к дезинфицирующим средствам с доказанной активностью против вирусов, имеющих оболочку, включая гипохлорит натрия (например, 0,1%-й для общей дезинфекции поверхности, перчаток), 62–71%-й этанол, 0,5%-я перекись водорода, четвертичные аммониевые соединения и фенольные соединения, если они используются в соответствии с рекомендациями производителя. Другие биоцидные агенты, такие как 0,05–0,2%-й хлорид бензалкония или 0,02%-й диглюконат хлоргексидина, могут быть менее эффективными [25].
Итальянские авторы сравнили вирулицидную активность против SARS-CoV следующих распространенных дезинфектантов:
• гипохлорит натрия 0,01% – 0,05% – 0,1%;
• этанол 70%;
• бензалкония хлорид 1%;
• хлоргексидин биглюконат 1%;
• 2-бензил-хлорфенол 2%;
• надуксусная кислота 0,035%.
Было показано, что SARS-CoV полностью инактивируется такими дезинфицирующими средствами, как надуксусная кислота, этанол 70%, гипохлорит натрия 0,05% и 0,1%, хлоргексидин биглюконат 1% и 2-бензил-хлорфенол 2% уже после обработки в течении 1 минуты. Для бензалкония хлорида требуется больше времени. При обработке биологических отходов (мокрота, выделения человека и т.п.) способность к разрушению вирусной РНК показали только 0,1%-й гипохлорит натрия и 2%-й 2-бензил-хлорфенол при времени контакта более 2 минут [26].
При сравнении известных антисептиков важно учитывать как их свойства, так и опыт применения, международные и национальные рекомендации (таблица). Для эффективного уничтожения SARS-CoV-2 ВОЗ рекомендованы два антисептика [25]: 70%-й раствор этанола и гипохлорит натрия.
Механизм действия гипохлорита натрия
Сильный бактерицидный эффект гипохлорита натрия связан со способностью продуцировать атомарный (активный) кислород. Гипохлорит натрия (NaOCl), полученный электрохимическим путем, расщепляется и выделяет активный кислород (O). Активный кислород повреждает бактериальные, вирусные и грибковые клеточные мембраны и повышает их проницаемость. Мембранане выдерживает осмотического давления, и патоген инактивируется. После того как кислород отделяется от гипохлорита натрия, вещество возвращается в свое естественное состояние воды и соли (NaCl). При таком механизме действия выработка резистентности не зарегистрирована [27, 28].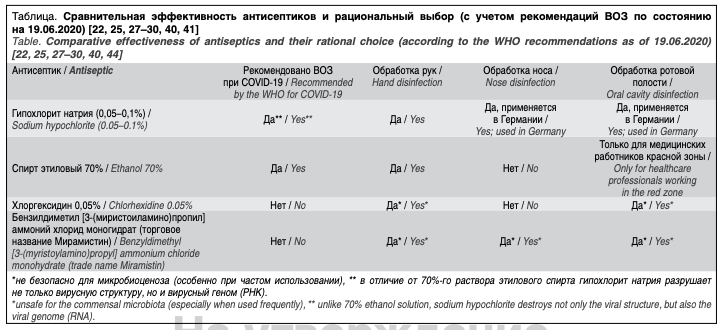
Гипохлорит натрия относится к антисептикам с умеренной вирулицидной активностью и входит в перечень средств дезинфекции, рекомендованных для предстерилизационной очистки и стерилизации, зарегистрированных в Российской Федерации [29, 30]. Средства на основе гипохлорита натрия обладают широкой антимикробной активностью, действуя на 99,9% основных возбудителей инфекционных болезней [31, 32, 33].
Спектр действия гипохлорита натрия включает различные патогены, в том числе вирусы герпеса 1-го и 2-го типа, аденовирус 8, цитомегаловирус, вирусы гепатита В и С, парвовирус, вирус гепатита А, вирусы гриппа, парагриппа, ротавирусы, RS-вирус, коронавирусы [34–45]. При применении гипохлорита натрия доказано уничтожение коронавирусов менее чем за 1 минуту [31].
Опыт применения гипохлорита натрия
Орошение носа солевыми растворами с гипохлоритом натрия рекомендовано для послеоперационного лечения взрослых пациентов с хроническим риносинуситом без полипов носа (рекомендации EPOS 2012, Европейский согласительный документ по риносинуситу и назальным полипам, 2012 (IIB) [40]. Также применение гипохлорита натрия включено в рекомендации EPOS 2020 [41].
Применение гипохлорита натрия апробировано среди 200 добровольцев: студенты в возрасте 19–22 лет, 70 из которых использовали спрей гипохлорита с концентрацией 0,03% (1-я группа), 70 – спрей гипохлорита натрия с концентрацией 0,06% (2-я группа), и 60 человек, составивших контрольную группу (3-я группа), распыляли изотонический раствор хлорида натрия в виде спрея. Спрей наносился 2 раза в день: утром (перед контактами с другими возможными носителями ОРВИ) и вечером в 17–20 ч (после контактов). Орошались миндалины и нос. Профилактику проводили в течение 20 дней. Орошение продолжали и при заболевании испытуемых, на фоне стандартного лечения ОРВИ. Исследовали тяжесть клинического течения инфекционного процесса у заболевших, состояние слизистых оболочек ротоглотки и миндалин. Применение спрея раствора гипохлорита натрия в концентрации 0,06% обеспечило снижение заболеваемости ОРВИ в 6 раз по сравнению с промыванием изотоническим раствором NaCl. Результаты исследования свидетельствуют о достоверном профилактическом действии спрея раствора гипохлорита натрия в отношении вирусов гриппа типа А, В, а также в отношении вирусов парагриппа и аденовирусов. Профилактическое и лечебное действия предлагаемого средства проявляются и в более легком течении заболевания ОРВИ, а также снижении числа осложнений у лиц, использующих спрей. Действие раствора гипохлорита натрия обусловлено не только его известными вирулицидными свойствами, но и способностью поддерживать мукозальный иммунитет ротоглотки, что выражается в повышении секреции IgA (SIgA) слюны. По-видимому, этот ранее не известный эффект является результатом антиоксидантных свойств гипохлорита натрия [38].
Клиническая эффективность применения гипохлорита натрия (NaOCl) в сочетании с физиологическим раствором для назального лаважа показана у пациентов с персистирующим риносинуситом, ассоциированным с ростом Staphylococcus aureus. Эндоназальное промывание 0,05%-м раствором NaOCl в физиологическом растворе подходит для длительного применения и, по-видимому, является хорошей альтернативой лаважу с одним физиологическим раствором при лечении симптоматических риносинуситов, связанных с рецидивирующими стафилококковыми инфекциями [39].
Гипохлорит натрия в концентрациях 0,1% и 0,06% широко применяется в хирургии, урологии и трансплантологии при лечении гнойных ран. Доказано повышение чувствительности микроорганизмов к антибактериальной терапии под воздействием гипохлорита натрия при лечении ожоговых ран. Известен способ лечения вторичной иммунной недостаточности при сепсисе и септическом шоке в урологии [43].
Имеется успешный опыт применения гипохлорита натрия в комплексном лечении сепсиса у пострадавших с политравмой [44], что важно для любых тяжелых пациентов отделений интенсивной терапии, включая случаи COVID-19.
Для медицинских целей в России гипохлорит натрия используется в качестве 0,06%-го раствора для внутриполостных инстилляций и наружного применения, а также раствора для инъекций. В хирургической практике он применяется для обработки, промывания или дренирования операционных ран и интраоперационной санации плевральной полости при гнойных поражениях; в акушерстве и гинекологии – для периоперационной обработки влагалища, лечения бартолинита, кольпита, трихомониаза, хламидиоза, эндометрита, аднексита и т. п.; в оториноларингологии – для полосканий носа и горла, закапывания в слуховой проход; в дерматологии – для влажных повязок, примочек, компрессов при различных видах инфекций [45].
Заслуживает внимания интересное исследование, которое было направлено на оценку клинической эффективности применения 0,05%-го раствора гипохлорита натрия для полоскания рта, его влияния на супрагингивальную биопленку и воспаление десен. Исследование проводилось в виде контролируемого рандомизированного слепого исследования параллельных групп у 40 заключенных тюрем. После подготовительного периода чистку зубов в течение 21 дня заменяли под контролем два раза в день полосканием 15 мл свежего раствора 0,05% гипохлорита натрия либо 15 мл дистиллированной воды. Клинические исходы оценивались с использованием индекса зубного налета Куигли–Хейна (QHPI), индекса десны и шелушения (L & SGI) и кровотечения при зондировании. На 21-й день средний показатель QHPI составлял 3,82 в группе с промыванием водой и 1,98 в группе с промыванием гипохлоритом натрия. Средний балл L & SGI составлял 2,1 в группе полоскания водой и 1,0 в группе полоскания гипохлоритом натрия, а средний процент участков, которые кровоточили при зондировании, составлял 93,1% в группе полоскания водой и 56,7% в группе полоскания гипохлоритом натрия. Различия были статистически значимы и достоверны (р = 0,001). Были сделаны выводы о том, что полоскание полости рта гипохлоритом натрия в концентрации 0,05% привело к значительному снижению воспаления десен и существенному уменьшению накопления наддесневой биопленки. Разбавленный гипохлорит натрия может представлять собой эффективный, безопасный и доступный антимикробный раствор для профилактики и лечения заболеваний пародонта [42].
Безопасность гипохлорита натрия
Исследования показывают, что гипохлорит натрия в концентрации 0,1% и менее безопасен, не является ни раздражителем кожи, ни сенсибилизатором [46].
Имеющиеся данные свидетельствуют о достаточно щадящем воздействии гипохлорита натрия на резидентную микробиоту [47].
Компания Alcavis провела тесты с их продуктом, содержащим 0,1%-й гипохлорит натрия. Было проведено сводное исследование на раздражение с использованием пластыря на 0,11%-м растворе гипохлорита натрия Amuchina, в дальнейшем именуемого Amu-Skin. В ходе исследования не наблюдалось клинически значимого раздражения. Отсутствовали признаки сенсибилизации к любому из продуктов, оцениваемых на этапе провокации. Компания Amuchina также провела повторную кожную аллергологическую пробу (тест TKL Laboratories). В условиях, применяемых в данном исследовании, с участием 194 добровольцев, отсутствовали признаки сенсибилизации к Amu-Skin или к носителю [48]. Миан и соавт. провели сравнительное клиническое исследование местных антисептиков при лечении ожоговых пациентов. Пациентов с ожогами лечили либо кремом с 1% сульфадиазина серебра (стандартное лечение), либо 0,05– 0,11%-м раствором гипохлорита натрия. Пациенты, получавшие раствор гипохлорита натрия, переносили лечение с меньшими проявлениями болевого синдрома, имели меньшую частоту возникновения дерматита и демонстрировали более быстрое заживление ран в сравнении с теми пациентами, которые получали крем сульфадиазина серебра [48].
Гнеми также исследовал развитие острого раздражения глаз гипохлоритом натрия. Исследование проводилось путем введения 0,1 мл 0,11%-го раствора гипохлорита натрия конъюнктивально кроликам. В течение 72-часового периода наблюдения не было отмечено никаких нежелательных реакций. Автор пришел к выводу, что 0,11%-й гипохлорит натрия не вызывает раздражения органа зрения у кроликов [48].
Быстрое разложение гипохлорита натрия после контакта с ранами, а также результаты исследования Заноло указывают на то, что в результате местного применения раствора гипохлорита натрия в кровотоке не будет обнаружен гипохлорит натрия или его минимальные количества [31].
Хасегава и соавт. исследовали влияние на крыс 104-недельного введения гипохлорита натрия в питьевой воде при концентрации 0,05–0,2%. Не наблюдалось значительного увеличения частоты развития каких-либо опухолей, что привело исследователей к выводу, что гипохлорит натрия не обладает канцерогенным потенциалом [31].
Вироксинол (МНН – гипохлорит натрия) – единственная серия в России для обработки носа, ротовой полости и рук, которая содержит активный компонент (гипохлорит натрия), включенный в рекомендации ВОЗ при COVID-19, имеющий доказательную базу по вирулицидному действию на коронавирусы (гипохлорит натрия уничтожает коронавирусы менее чем за 1 минуту за счет активного кислорода), а также опыт клинического применения обработки носовой и ротовой полости при различных нозологиях. Вироксинол представлен в виде спрей-геля для носа, раствора для полости рта, геля для рук. Активным компонентом серии Вироксинол является гипохлорит натрия в концентрации 0,1% и менее (в зависимости от формы выпуска), полученный электрохимическим путем (т.е. без использования хлора). При попадании на кожу гипохлорит натрия разрушается с образованием атомарного кислорода, обладающего вирулицидным и антибактериальным действием, и NaCL. 
В организме человека гипохлорит натрия – активный естественный компонент мононуклеаров (моноцитов и микрофагов (нейтрофилов)) – клеток иммунной системы человека, которые вырабатывают небольшое количество гипохлорита натрия, участвующего в процессе фагоцитоза, который используется для переваривания бактерий и вирусов и не уступает пероксидным соединениям. Микробицидная активность значительно возрастает в присутствии анионов галогенов [49].
Выводы
Среди рекомендованных ВОЗ антисептиков, которые эффективны в отношении широкого спектра респираторных вирусных инфекций, включая вирусы гриппа, риновирусы, SARS-CoV-2, средствами выбора являются 70%-й раствор этилового спирта и гипохлорит натрия.
Гипохлорит натрия широко используется в клинической практике как вирулицидное и антибактериальное средство и в качестве антисептика включен в клинические рекомендации по лечению риносинуситов (EPOS 2012, 2020). ции по лечению риносинуситов (EPOS 2012, 2020).
Применение спрея раствора гипохлорита натрия в концентрации 0,06% обеспечило снижение заболеваемости ОРВИ в 6 раз по сравнению с использованием промывания изотоническим раствором NaCl.
Вироксинол – единственный в России гипохлорит натрия, который может использоваться как для профилактики, так и для комбинированной терапии респираторных инфекций в условиях пандемии COVID-19 как в медицинских учреждениях, так и для домашнего использования в качестве безопасного антисептика.
В связи с пандемией COVID-19 проводятся дополнительные более масштабные исследования по изучению эффективности и возможности применения раствора гипохлорита натрия в клинической практике. В целом применение гипохлорита натрия локально является не только рекомендованным медицинским сообществом, но и соответствует требованиям высокой эффективности и безопасности, что крайне важно для профилактики новых заражений в условиях пандемии COVID-19, эпидемий гриппа и подъема сезонной заболеваемости ОРВИ, принимая во внимание достаточно большое число бессимптомных или малосимптомных носителей вирусов.
Информация о финансировании
Данная работа подготовлена при поддержке компании ООО «ИНТЕЛБИО».
Financial support
Financial support has been provided for this work by Intelbio LLC.
Конфликт интересов
Автор заявляет об отсутствии конфликта интересов.
Conflict of interests
The author declare that there is not conflict of interests.
Литература
1. Руководство по вирусологии. Под ред. академика РАН Д.К.Львова. МИА, 2013.
2. Викулов ГХ. Частые ОРВИ и грипп в практике врача терапевта, педиатра и оториноларинголога: современная диагностика и лечение с позиции доказательной медицины. Consilium Medicum. 2015;17(11):47-50.
3. Викулов ГХ. Новые и возвращающиеся респираторные вирусные инфекции: алгоритмы диагностики и терапии. РМЖ. Медицинское обозрение. 2018; 8(1):5-11.
4. Викулов ГХ. Новые и возвращающиеся респираторные вирусные инфекции: алгоритмы диагностики, способы терапии и профилактики. Медицина (Алматы). 2019;7-8(205-206):53-64. DOI: 10.31082/1728-452X-2019-205-206- 7-8-53-64
5. https://coronavirus.jhu.edu/map.html. Дата обращения 19.06.2020.
6. Сперанская АА. Лучевые проявления новой коронавирусной инфекции COVID-19. Лучевая диагностика и терапия. 2020;11(1):18-25. DOI: 10.22328/ 2079-5343-2020-11-1-18-25
7. Чучалин АГ. Пневмония: актуальная проблема современной медицины. Materia Medica. 1995;4:5-10.
8. Синопальников АИ. Внебольничная пневмония у взрослых. Consilium medicum. 2007;9(3):5-16.
9. Новиков ЮК. Внебольничные пневмонии. Русский медицинский журнал. 1999;7(17):825-829.
10. Griffin MR, Zhu Y, Moore MR, Whitney CG, Grijalva CG. U.S. hospitalizations for pneumonia after a decade of pneumococcal vaccination. N Engl J Med. 2013; 369(2):155-163. DOI: 10.1056/NEJMoa1209165
11. International Committee of Taxonomy of Viruses. https://talk.ictvonline.org/taxonomy
12. Coronavirus disease (COVID-19) outbreak. WHO. https://www.who.int/ emergencies/diseases/novel-coronavirus-2019
13. Горенков ДВ, Хантимирова ЛМ, Шевцов ВА, Рукавишников АВ, Меркулов ВА, Олефир ЮВ. Вспышка нового инфекционного заболевания COVID-19: β-коронавирусы как угроза глобальному здравоохранению. БИОпрепараты. Профилактика, диагностика, лечение. 2020;20(1):6-20. DOI: 10.30895/2221- 996X-2020-20-1-6-20
14. Никифоров ВВ, Суранова ТГ, Чернобровкина ТЯ, Янковская ЯД, Бурова СВ. Новая коронавирусная инфекция (COVID-19): клинико-эпидемиологические аспекты. Архивъ внутренней медицины. 2020;10(2):87-93. DOI: 10.20514/2226- 6704-2020-10-2-87-93
15. Yi Y, Lagniton PNP, Ye S, Li E, Xu RH. COVID-19: what has been learned and to be learned about the novel coronavirus disease. Int J Biol Sci. 2020 Mar 15; 16(10):1753-1766. DOI: 10.7150/ijbs.45134
16. Ji W, Wang W, Zhao X, Zai J, Li X. Cross-species transmission of the newly identified coronavirus 2019-nCoV. J Med Virol. 2020;92(4):433-440. DOI: 10.1002/ jmv.25682
17. Mady LJ, Kubik MW, Baddour K, Snyderman CH, Rowan NR. Consideration of povidone-iodine as a public health intervention for COVID-19: Utilization as "Personal Protective Equipment" for frontline providers exposed in high-risk head and neck and skull base oncology care. Oral Oncol. 2020 Jun;105:104724. DOI: 10.1016/j.oraloncology.2020.104724
18. Keyes M, Thibodeau R. Dakin Solution (Sodium Hypochlorite). StatPearls Publishing; 2020.
19. Peng X, Xu X, Li Y, Cheng L, Zhou X, Ren B. Transmission routes of 2019-nCoV and controls in dental practice. Int J Oral Sci. 2020 Mar 3;12(1):9. DOI: 10.1038/ s41368-020-0075-9
20. Ramalingam S, Cai B, Wong J, et al. Antiviral innate immune response in nonmyeloid cells is augmented by chloride ions via an increase in intracellular hypochlorous acid levels. Sci Rep. 2018;8(1):13630. Published 2018 Sep 11. DOI: 10.1038/s41598-018-31936-y
21. Временные методические рекомендации. Профилактика, диагностика и лечение новой коронавирусной инфекции (COVID-19). Версия 6, 7 (28.04.2020, 03.06.2020).
22. Шестопалов НВ, Пантелеева ЛГ, Соколова НФ, Абрамова ИМ, Лукичев СП. Федеральные клинические рекомендации по выбору химических средств дезинфекции и стерилизации для использования в медицинских организациях. Москва, 2015.
23. Васильев АН, Карпов АН, Сакварелидзе СН. Спрей для экстренной профилактики острых респираторных инфекций. Патент на изобретение. 05.09.2018.
24. Орлова ОА, Акимкин ВГ. Профилактика внутрибольничных пневмоний в отделении хирургической реанимации. Сеченовский вестник. 2016;1(23):24-30.
25. Временное руководство Всемирной Организации Здравоохранения от 17 марта 2020 г. «Уход на дому за пациентами с COVID-19 с легкими симптомами и мониторинг контактных лиц». Доступ: https://base.garant.ru/73861132/
26. Ansaldi F, Banfi F, Morelli P, Valle L, Durando P, Sticchi L, et al. SARS-CoV, influenza A and syncitial respiratory virus resistance against common disinfectants and ultraviolet irradiation. Journal of Preventive Medicine and Hygiene. 2004; 45(1-2):5-8.
27. List N: Products with Emerging Viral Pathogens AND Human Coronavirus claims for use against SARS-CoV-2 Date Accessed: 04/26/2020, www.epa.gov/pesticideregistration/list-n-disinfectants-use-against-sars-cov-2
28. COVID-19: EPA RELEASES LIST OF REGISTERED DISINFECTANTS. Access: https://www.healthleadersmedia.com/covid-19/covid-19-epa-releases-listregistered-disinfectants
29. Герасимов ВН, Лущиков СБ, Бабич ИВ, и др. Антимикробные и дезинфицирующие свойства двух хлорактивных дезинфектантов: усовершенствованного гипохлорита натрия и двуосновной соли гипохлорита кальция. Дезинфекционное дело. 1999;4:10-18.
31. Kampf G, Todt D, Pfaender S, Steinmann E. Persistence of coronaviruses on inanimate surfaces and their inactivation with biocidal agents. J Hosp Infect. 2020 Mar;104(3):246-251. DOI: 10.1016/j.jhin.2020.01.022
32. Croughan WS, Behbehani AM. Comparative study of inactivation of herpes simplex virus types 1 and 2 by commonly used antiseptic agents. J Clin Microbiol. 1988 Feb;26(2):213-5.
33. Nagington J, Sutehall GM, Whipp P. Tonometr disinfection and viruses. British Journal of Ophthalmology. 1983;67:674-676.
34. Hunter DT. Sodium hypochlorite in the treatment of herpes simplex virus infections. Cutis. 1983;31(3):328-332.
35. Гинтер ЕК. Способ лечения хронической генерализованной вирусной инфекции. Патент на изобретение. 10.09.1997.
36. Мязин РГ, Емельянов ДН. Оценка детоксицируюших и противовирусных свойств гипохлорита натрия при лечении вирусных гепатитов В и С. Медицинских альманах. 2013;3(27):145-147.
37. Coronavirus infection. Coronavirus infection and pregnancy. Information for pregnant women and their families. Royal college of Obstetricians & Gynaecologists; 2020. Access: https://www.rcog.org.uk/en/guidelines-research-services/guidelines/ coronavirus-pregnancy/ covid-19-virus-infection-and-pregnancy/
38. Карпов АН, Васильев АН, Сакварелидзе СН. Спрей для экстренной профилактики острых респираторных вирусных инфекций. Патент на изобретение № 2665959 от 21.11.2017. https://findpatent.ru/patent/266/2665959.html
39. Raza T, Elsherif HS, Zulianello L, Plouin-Gaudon I, Landis BN, Lacroix JS. Nasal lavage with sodium hypochlorite solution in Staphylococcus aureus persistent rhinosinusitis. Rhinology. 2008;46(1):15-22.
40. Fokkens WJ, Lund VJ, Mullol J, Bachert C, Alobid I, Baroody F, et al. European Position Paper on Rhinosinusitis and Nasal Polyps 2012. Rhinol Suppl. 2012 Mar(23):1-298.
41. Fokkens WJ, Lund VJ , Hopkins C, Hellings PW, Kern R, Reitsma S, et al. European Position Paper on Rhinosinusitis and Nasal Polyps 2020 Rhinology. 2020 Suppl. 29:1-464.
42. De Nardo R, Chiappe V, Gómez M, Romanelli H, Slots J. Effects of 0.05% sodium hypochlorite oral rinse on supragingival biofilm and gingival inflammation. Int Dent J. 2012;62(4):208-212. DOI: 10.1111/j.1875-595X.2011.00111.x
43. Кирпатовский ВИ, Перепанова ТС, Чернышев ИВ, Иващенко АВ, Иващенко ВВ, Надточий ОН, Аполихин ОИ, Кудрявцев ЮВ. Способ лечения вторичной иммунной недостаточности при сепсисе и септическом шоке в урологии. Патент на изобретение № 2586243.RU.С1.10.06.2016. https://findpatent.ru/ patent/258/2586243.html
44. Гурьев СЕ, Танасиенко ПВ, Палагнюк КВ. Возможности гипохлорита натрия в комплексном лечении сепсиса у пострадавших с политравмой. Экстренная медицина. 2017;6(1):122-127.
45. Натрия гипохлорит. Справочник лекарств РЛС. Регистр лекарственных средств России РЛС.
46. A Look at COVID 19 in Terms of: 1. Respiratory Protection. DOI: 10.13140/ RG.2.2.26737.02405
47. Burnham CA, Hogan PG, Wallace MA, et al. Topical Decolonization Does Not Eradicate the Skin Microbiota of Community-Dwelling or Hospitalized Adults. Antimicrob Agents Chemother. 2016;60(12):7303-7312. Published 2016 Nov 21. DOI: 10.1128/AAC.01289-16
48. Bruch MK. Toxicity and safety of topical sodium hypochlorite. Contrib Nephrol. 2007;154:24-38. DOI: 10.1159/000096812
49. Petrosian EA, Laĭpanov IM. Vliianie natriia gipokhlorita na khemiliuminestsentsiiu neĭtrofil'nykh granulotsitov pri lechenii gnoĭno-vospalitel'nykh zabolevaniĭ organov zabriushinnogo prostranstva [Effect of sodium hypochlorite on neutrophilic granulocytes during treatment for purulent-inflammatory diseases of retroperitoneal organs]. Urologiia. 2002;(2):32-34. (In Russian).
50. Kramer A. Wundantiseptik. ARS MEDICI. 2016;9:419-426.
51. Lorberth J, Massa W. Zu den chemischen Grundlagen der Wirkung von Steralythen. Wund Management. 2012;3:52-54.
References
1. Rukovodstvo po virusologii. Pod red. akademika RAN D.K.L'vova. MIA, 2013. (In Russian).
2. Vikulov GKh. Chastye ORVI i gripp v praktike vracha terapevta, pediatra i otorinolaringologa: sovremennaya diagnostika i lechenie s pozitsii dokazatel'noi meditsiny. Consilium Medicum. 2015;17(11):47-50. (In Russian).
3. Vikulov GH. New and reemerging respiratory viral infections: diagnostic and therapeutic algorithms. RMJ. Medical Review. 2018;8(1):5–11. (In Russian).
4. Vikulov GKh. Emerging and reemerging respiratory viral infections: algorithms of diagnostics, approaches of prophylaxis and therapy. Meditsina (Almaty) (Medicine (Almaty)). 2019;7-8(205-206):53-64. DOI: 10.31082/1728-452X-2019-205-206- 7-8-53-64 (In Russian).
5. https://coronavirus.jhu.edu/map.html. Link available 19.06.2020.
6. Speranskaya AA. Radiological signs of a new coronavirus infection COVID-19. Diagnostic radiology and radiotherapy. 2020;11(1):18-25. DOI: 10.22328/2079- 5343-2020-11-1-18-25 (In Russian).
7. Chuchalin AG. Pnevmoniya: aktual'naya problema sovr7. Chuchalin AG. Pnevmoniya: aktual'naya problema sovremennoi meditsiny. Materia Medica. 1995;4:5–10. (In Russian).
8. Sinopal'nikov AI. Vnebol'nichnaya pnevmoniya u vzroslykh. Consilium medicum. 2007;9(3):5–16. (In Russian).
9. Novikov YuK. Vnebol'nichnye pnevmonii. Medical Journal of the Russian Federation (Russian Medical Journal). 1999;7(17): 825–829. (In Russian).
10. Griffin MR, Zhu Y, Moore MR, Whitney CG, Grijalva CG. U.S. hospitalizations for pneumonia after a decade of pneumococcal vaccination. N Engl J Med. 2013; 369(2):155-163. DOI: 10.1056/NEJMoa1209165
11. International Committee of Taxonomy of Viruses. https://talk.ictvonline.org/ taxonomy
12. Coronavirus disease (COVID-19) outbreak. WHO. https://www.who.int/emergencies/diseases/novel-coronavirus-2019
13. Gorenkov DV, Khantimirova LM, Shevtsov VA, Rukavishnikov AV, Merkulov VA, Olefir YuV. An Outbreak of a New Infectious Disease COVID-19: β-coronaviruses as a Threat to Global Healthcare. BIOpreparations. Prevention, Diagnosis, Treatment. 2020;20(1):6-20. DOI: 10.30895/2221-996X-2020-20-1-6-20 (In Russian).
14. Nikiforov VV, Suranova TG, Chernobrovkina TYu, Yankovskaya YD, Burova SV. New Coronavirus Infection (Covid-19): Clinical and Epidemiological Aspects. The Russian Archives of Internal Me
Вам также может быть интересно