Экзема: тактика выбора наружной терапии
2021.03.18Заславский Д. В.1 , Туленкова Е. С.1 , Монахов К. Н.2 , Холодилова Н. А.2 , Кондратьева Ю. С.3 , Тамразова О. Б.4 , Немчанинова О. Б.5 , Гулиев М. О.6 , Шливко И. Л.7,*, Торшина И. Е.8
1 Санкт-Петербургский государственный педиатрический медицинский университет Министерства здравоохранения Российской Федерации 194100, Российская Федерация, г. Санкт-Петербург, ул. Литовская, д. 2
2 Первый Санкт-Петербургский государственный медицинский университет им. академика И. П. Павлова Министерства здравоохранения Российской Федерации 197022, Российская Федерация, г. Санкт-Петербург, ул. Льва Толстого, д. 6–8
3 Алтайский государственный медицинский университет Министерства здравоохранения Российской Федерации 656038, Российская Федерация, г. Барнаул, пр-т Ленина, д. 40
4 Российский университет дружбы народов 117198, Российская Федерация, г. Москва, ул. Миклухо-Маклая, д. 6
5 Новосибирский государственный медицинский университет Министерства здравоохранения Российской Федерации 630091, Российская Федерация, г. Новосибирск, Красный проспект, д. 52
6 Кабардино-Балкарский государственный университет им. Х. М. Бербекова 360004, Российская Федерация, г. Нальчик, ул. Чернышевского, д. 173
7 Приволжский исследовательский медицинский университет Министерства здравоохранения Российской Федерации 603005, Российская Федерация, г. Нижний Новгород, пл. Минина и Пожарского, д. 10/1
8 Смоленский государственный медицинский университет Министерства здравоохранения Российской Федерации 214019, Российская Федерация, г. Смоленск, ул. Крупской, д. 28
Лечебные эффекты синтетических танинов основаны на их вяжущем действии, а также противозудном, противомикробном и противовоспалительном эффектах. Материалы и методы. Клиническое исследование препаратов Неотанин спрея, лосьона (суспензии) и крема проводилось в 8 клинических центрах с июня 2017 г. по январь 2018 г. Данное исследование было открытым несравнительным. В исследование было включено 68 пациентов обоего пола в возрасте от 1 месяца до 80 лет с экзематозными дерматозами, в стадии обострения с мокнутием, в том числе осложненные вторичной инфекцией (включая локализацию элементов на лице). Перед включением пациентов в исследование был изучен анамнез, демографические данные, сопутствующие заболевания, данные физикального обследования. Схема назначения препарата включала два этапа: 1-й этап: на 1–5 дней назначался спрей или лосьон (суспензия) Неотанин 3–4 раза в сутки — до полного подсушивания элементов; 2-м этапом назначался крем Неотанин 3 раза в сутки до исчезновения клинических проявлений дерматоза на коже. Длительность исследования составила от 5 до 14 дней, по мере наступления ремиссии, пациенты завершали участие в исследовании. Критериями эффективности исследуемого препарата являлись динамика субъективных жалоб, объективная оценка состояния пациента (наличие и выраженность клинических симптомов), динамика ДИКЖ. Результаты. Препараты Неотанин показали высокую эффективность в острую и подострую стадию воспалительного процесса в качестве противозудного средства. Зуд купировался в течение 5 минут после нанесения препаратов, противозудный эффект длился в среднем 3–4 часа. Уже на 3-й день выраженные экскориации отсутствовали у 85 % пациентов. Неотанин продемонстрировал выраженное противовоспалительное действие. Через неделю применения симптомы эритемы и отечности регрессировали у 92 % пациентов, достоверно уменьшились проявления воспалительной экссудации, уже через неделю мокнутие отсутствовало у 100 % пациентов. Отсутствие серьезных нежелательных эффектов у пациентов за время наблюдения свидетельствует о хорошей переносимости и безопасности данного препарата.
Ключевые слова: экзематозные дерматозы, синтетический танин, полидоканол, противозудный эффект
Конфликт интересов: авторы заявляют об отсутствии потенциального конфликта интересов, требующего раскрытия в данной статье.
Для цитирования: Заславский Д. В., Туленкова Е. С., Монахов К. Н., Холодилова Н. А., Кондратьева Ю. С., Тамразова О. Б., Немчанинова О. Б., Гулиев М. О., Шливко И. Л., Торшина И. Е. Экзема: тактика выбора наружной терапии. Вестник дерматологии и венерологии. 2018;94(3):56–66. https://doi.org/10.25208/0042-4609- 2018-94-3-56-66
Введение
Экзема (eczema; греч. eczeo — «вспыхивать», «вскипать», «пузыриться») — своеобразное воспалительное заболевание кожи, начинающееся, как правило, остро, но затем принимающее обычно хроническое рецидивирующее течение (Павлов С. Т., 1969) [1].
Экзема — хроническое эритематозно-везикулярное заболевание кожи, развивающееся на фоне особых изменений ее реактивности (Самцов А. В., 2008) [2].
Экзема не имеет единой этиологии и представляет собою типичную кожную реакцию, которая может быть вызвана воздействием на кожу разнообразных внешних факторов, но развивающуюся лишь при наличии своеобразных изменений реактивности кожи. Патогенез экземы не является до настоящего времени окончательно установленным.
«Самое непостоянное в экземе вообще — это ее течение» (Дарье Ж., 1930) [3]. Следовательно, можно перефразировать это определение, что экзема всегда возвращается! Экзема — самое частое полиморфное заболевание, которое всегда можно вызвать искусственно на первом попавшемся индивидууме (Гебра Ф., 1864). Ф. Гебра на вопрос «Что такое экзема?» ответил: «Экзема — это то, что выглядит как экзема» [4]. «Больной экземой — это трясина, в которой барахтается множество дерматологов, и неудивительно, что некоторые аллергологи и иммунологи, пытающиеся сюда ступить, уже начали ощущать зыбкость почвы под ногами (Sulzberger and Goodman, 1936) [5]. «Если вы знаете причину, это не экзема; если вы не знаете причину, тогда это она и есть» (Malcolm A. Morris, 1903) [6]. Большинство отечественных дерматологов считает экзему самостоятельным воспалительным дерматозом, обусловленным серозным воспалением преимущественно сосочкового отдела дермы и очаговым спонгиозом шиповатого слоя эпидермиса, проявляющимся полиморфной зудящей сыпью.
В современной западной дерматологии термин «экзема» используется для обозначения неспецифической, не имеющей нозологической самостоятельности воспалительной реакции кожи, патоморфологически характеризующейся спонгиозом, неравномерным акантозом и поверхностным периваскулярным инфильтратом, состоящим преимущественно из лимфоцитов и гистиоцитов («спонгиотический дерматит»). Многие современные западные дерматологии используют термины «дерматит» и «экзема» как синонимы. Для верификации диагноза необходимо гистологическое исследование, при котором может обнаруживаться неспецифическое воспаление эпидермиса с наличием спонгиоза (спонгиотическая модель воспаления).
Спонгиоз является относительно неспецифическим морфологическим состоянием, наблюдающимся при множестве дерматозов, но особенно часто при так называемых «экзематозных дерматитах»: экземе (эндогенном дерматите), атопическом дерматите, контактном аллергическом и ирритантном дерматите.
Спонгиотическая воспалительная реакция характеризуется интраэпидермальным межклеточным отеком (спонгиозом) эпидермиса. В ранних стадиях наблюдается расширение межклеточных промежутков шиповатых кератиноцитов, но целостность эпидермиса сохраняется. В поздних стадиях происходит разделение кератиноцитов и возникают спонгиотические полости.
Очаги спонгиоза могут проявляться микроскопическими или клинически видимыми пузырьками, микроскопическими полостями. В большинстве случаев специфический гистологический диагноз при наличии спонгиоза в эпидермисе невозможен; морфолог может диагностировать «неспецифическое воспаление кожи с явлениями спонгиоза».
Очаги спонгиоза часто весьма вариабельны, множественны и сочетаются с внутриклеточным отеком и экзоцитозом воспалительных клеток. Иногда в очагах спонгиоза имеются гранулоциты (эозинофилы или нейтрофилы), или процесс распространяется в придатки кожи (фолликулярный спонгиоз).
Согласно современным данным важную роль в патогенезе спонгиоза играют Т-лимфоциты, инфильтрирующие кожу. Эти Т-лимфоциты секретируют провоспалительные цитокины и индуцируют апоптоз кератиноцитов с помощью killer molecules, что последовательно приводит к расщеплению адгезивных молекул, включая Е-кадхерин на поверхности кератиноцитов. Накопление межклеточной жидкости приводит к расширению пространства между кератиноцитами, создавая внешнее сходство гистологической картины с губкой [1, 2].
По течению спонгиотический дерматит подразделяется на острую, подострую и хроническую стадии.
Острый спонгиотический дерматит при гистологическом исследовании характеризуется выраженным межклеточным отеком с образованием микрополостей и даже макрополостей в шиповатом слое эпидермиса (последние клинически проявляются микровезикулами). Шиповатые кератиноциты, окружающие эпидермальные полости, имеют звездчатую форму, и в результате межклеточного отека этот слой эпидермиса приобретает своеобразный «губчатый» вид (отсюда термин «спонгиоз»). Роговой слой эпидермиса остается нормальным, паракератоза нет. Сопутствующими симптомами являются отек сосочкового слоя дермы и поверхностный периваскулярный воспалительный инфильтрат, состоящий из лимфоцитов и гистиоцитов, иногда эозинофилов; возможны экзоцитоз лимофоцитов в спонгиотические полости и экстравазаты эритроцитов. Клиническая картина отражает указанные выше гистологические изменения и проявляется микровезикулами и отдельными вскрывшимися пузырьками (серозные «колодцы» Девержи).
Подострый спонгиотический дерматит при гистологическом исследовании представлен спонгиозом с формированием микрополостей в эпидермисе, над которыми отмечается очаговый паракератоз, иногда выявляется умеренный акантоз. Паракератотические участки эпидермиса могут содержать коагулированную плазму со скоплениями лимфоцитов и нейтрофилов, формирующими корки. Импетигинизация за счет грам-положительных кокков (стафилококков и стрептококков) может сопровождаться появлением в инфильтрате нейтрофилов. В дерме отмечается поверхностный периваскулярный околососудистый инфильтрат, состоящий из лимфоцитов и гистиоцитов, иногда встречаются эозинофилы. Отек сосочкового слоя дермы выражен слабо. Клиническая картина этих высыпаний представлена розовыми или красными, шелушащимися папулами и бляшками, часто осложненными экскориациями. Большинство подострых высыпаний спонгиотического дерматита принимают хроническое течение (например, лихенизированные папулы и бляшки при атопическом дерматите).
Хронический спонгиотический дерматит клинически проявляется лихенизацией. При гистологическом исследовании выявляется компактный гиперкератоз, акантоз с гипергранулезом, спонгиоз, иногда фиброз сосочкового слоя дермы, обусловленный хроническим расчесыванием кожи. Спонгиоз обычно выражен слабо и имеет очаговый, часто фолликулярный характер. Лимфоциты, часто в сочетании с клетками Лангерганса, являются наиболее характерными воспалительными клетками, идентифицируемыми в спонгиотическом эпидермисе. В некоторых случаях в очагах спонгиоза преобладают эозинофилы (эозинофильный спонгиоз) и/или нейтрофилы (нейтрофильный спонгиоз). При выявлении этих типов спонгиоза, особенно нейтрофильного, необходимо использовать PAS-реакцию для выявления дерматофитов. Клиническая картина «экзематозных» дерматозов весьма полиморфна, зависит от длительности заболевания, этиологии и локализации, а также наличия экскориаций. В состоянии ремиссии клинические и морфологические изменения обычно ограничиваются эпидермисом. Первичными и вторичными патологическим изменениями эпидермиса являются эритема, везикулы, чешуйки, корки, лихенизация, гиперпигментация, экскориации, мокнутие, эрозии и трещины. Очаги поражения при спонгиотических дерматитах не имеют четких границ (за исключением нумулярной экземы и контактного дерматита).

Спектр дерматозов, характеризующихся экссудативным воспалением [3]:
• Экзематозные дерматозы;
• Атопический дерматит;
• Аллергический контактный дерматит;
• Простой контактный дерматит;
• Фотодерматиты;
• Экзема микровезикулярная ладоней и подошв (дисгидротический дерматит);
• Экзема бляшечная (нумуллярный дерматит);
• Экзема (дерматит) застойная (Stasis dermatitis);
• Простой хронический лихен Видаля;
• Узловатое пруриго;
• Аутосенсибилизация или id-реакции (экзематид);
• Себорейный дерматит;
• Спонгиотическая («экзематоидная») реакция лекарственной гиперчувствительности;
• Розовый питириаз;
• Себорейный дерматит;
• Эритродермии.
Топическая терапия указанных выше дерматозов наряду с системным подходом в лечении имеет большое значение для регресса воспалительного экссудативного процесса, обеспечивая контроль за сопутствующими этому воспалению субъективными симптомами (зуд, жжение).
Наружное лечение традиционно принято проводить в зависимости от клинической стадии процесса. При мокнутии применяются максимально поверхностно действующие топические препараты в виде примочек, влажно-высыхающих повязок с вяжущими средствами. В подострую стадию осуществляется переход на кремы, пасты и мази.
Вяжущие вещества сотни лет применяли для медицинских целей (рис. 1–3). Сегодня эти средства не утратили своей актуальности, являясь необходимым компонентом лечения больных дерматологического профиля. Благодаря вяжущему эффекту танины природного и синтетического происхождения широко применяют в комплексной терапии воспалительных заболеваний кожи.
До 1950-х годов использовали танины только природного происхождения. Экстракты из коры дуба назначали больным, например, при повышенной потливости стоп или воспалительных процессах в полости рта. Синтетический танин, полифенольный сложный препарат, был разработан в середине прошлого столетия. Танины действуют путем связывания структурных белков. Эти соединения образовываются между аминогруппами, в основном щелочных аминокислот (аргинин, лизин) полипептидов и протеинов экссудата и фенольной гидроксильной группы синтетического танина.
Подсушивающие свойства синтетического танина обеспечиваются тонкой коагуляционной пленкой, которая образуется слоем химически связанных в сеть протеинов, что приводит к объединению коллоидных тканей верхних слоев кожи [4]. Преципитация протеинов, обусловленная местным применением танинов, определяет утолщение коллоидных структур с последующим уплотнением и стабилизацией клеточных мембран, уменьшением экссудации тканевой жидкости. Благодаря химико-физическому образованию этой тонкой когерентной защитной коагуляционной мембраны синтетические танины могут подсушивать мокнущую кожу и уменьшать зуд [5].
Противозудные свойства синтетических танинов были выявлены путем проведения экспериментальных проб in vitro и тестовых методик. Пушман и Мэтфис (Puschmann и Matthies) [6] доказали противозудный эффект танина методом гистамино-волдырного теста и методом стимуляции слизистой оболочки губ. Гистамино-волдырный тест был проведен на 85 здоровых добровольцах]. Помимо вяжущего и противозудного, синтетический танин обладает противовоспалительным [7, 8], противомикробным действиями, уменьшает трансэпидермальную потерю воды.
Синтетический танин имеет существенные преимущества перед природными аналогами благодаря очистке действующего вещества от возможных примесей, точности дозирования, контролю качества на всех этапах производства и более длительному сроку годности. Благодаря высокому профилю безопасности они широко применяются у младенцев и детей. Системное действие у препарата отсутствует [9]. Кроме того, применение синтетического танина не приводит к таким отрицательным моментам, как окраска ванн, одежды и самой кожи при использовании [10].
В России синтетический танин доступен только в виде фенол сульфоната натрия, который выпускается под торговым названием Неотанин, представлен в трех формах: спрей, лосьон (суспензия), крем. Основными активными компонентами серии препаратов Неотанин являются синтетический танин и полидоканол. В форму лосьона, помимо синтетического танина и полидоканола, включен оксид цинка.
Активным компонентом серии препаратов Неотанин является полидоканол, который обладает противозудным действием. Противозудный эффект полидоканола развивается через 5–10 минут после нанесения на кожу, длительность действия составляет в среднем 3–4 часа. Полидоканол способен усиливать вяжущее, подсушивающее действие танина, способствует заживлению эрозий, обладает анестезирующим действием на кожу и слизистые, снижает чувствительность и проводимость чувствительных нервов.
Цели исследования серии препаратов Неотанин: 1) оценка эффективности и безопасности препаратов Неотанин спрея, лосьона (суспензии) и крема у пациентов с экзематозными дерматозами с учетом динамики изменений субъективных, объективных признаков, ДИКЖ (Дерматологический Индекс Качества Жизни); 2) оценка сроков разрешения клинических проявлений экзематозных дерматозов с использованием исследуемых препаратов серии Неотанин.
Материалы и методы
Клиническое исследование препаратов Неотанин спрея, лосьона (суспензии) и крема проводилось в 8 клинических центрах с июня 2017 г. по январь 2018 г.
Данное исследование было открытым несравнительным. В исследование было включено 68 пациентов обоего пола в возрасте от 1 месяца до 80 лет с экзематозными (спонгиотическими) дерматозами, в стадии обострения с мокнутием, в том числе осложненные вторичной инфекцией (включая локализацию элементов на лице). В исследование были включены пациенты, находящиеся на амбулаторном и стационарном лечении: 28 мужчин (от 1 месяца до 80 лет) и 40 женщин (от 5 месяцев до 79 лет), среди которых 21 беременная (возраст от 20 до 40 лет). Диагностика дерматозов основывалась на комплексной оценке клинико-анамнестических и лабораторных данных.
Характеристика пациентов, включенных в исследование по нозологическим формам дерматозов (табл. 1).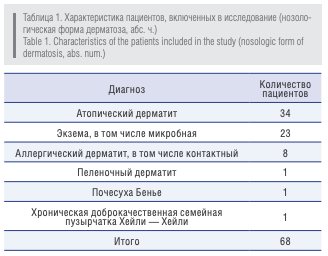
Давность заболевания у пациентов составила от 1 месяца до 79 лет. Перед включением пациентов в исследование был изучен анамнез, демографические данные, сопутствующие заболевания, данные физикального обследования. При включении в исследование все больные предъявляли жалобы на зуд, жжение кожных покровов и бессонницу — 68 (100 %) пациентов (у детей первого года жизни отмечалось беспокойство и нарушение сна). Схема назначения препарата включала два этапа: 1-й этап — на 1–5 дней назначался спрей или лосьон (суспензия) Неотанин 3–4 раза в сутки — до полного подсушивания элементов; 2-м этапом назначался крем Неотанин 3 раза в сутки до исчезновения клинических проявлений дерматоза на коже. Длительность исследования составила от 5 до 14 дней, включала 5 визитов (для амбулаторных больных). По мере наступления ремиссии пациенты завершали участие в исследовании. При каждом визите оценивались жалобы пациента и клиническая картина заболевания. Часть пациентов дополнительно получала сопутствующую терапию: энтеросорбенты, десенсибилизирующие средства, системные антигистаминные, наружно — эмоленты. В ходе исследования не допускалось назначение топических и системных глюкокортикостероидов и антибактериальных препаратов, топических антигистаминных препаратов и антисептиков. Оценка субъективных клинических признаков (жалобы пациента) проводилась по следующим показателям: патологические элементы на коже, зуд кожных покровов, жжение, бессонница. Для оценки степени поражения кожных покровов использовались следующие объективные признаки воспаления: эритема, отек, корки/мокнутие, экскориации, лихенификация, сухость кожи, трещины/эрозии. Интенсивность каждого признака (субъективного и объективного) оценивалась по четырехуровневой шкале: 0 — отсутствие, 1 — слабая, 2 — умеренная, 3 — сильная.
Критериями эффективности исследуемого препарата являлись: динамика субъективных жалоб, объективная оценка состояния пациента (наличие и выраженность клинических симптомов), динамика ДИКЖ. Для оценки эффективности терапии на первом этапе лечения — оценки уменьшения признаков экссудативного воспаления — использовались следующие критерии.
1. Выраженное улучшение: прекращение мокнутия, полное подсушивание элементов, уменьшение гиперемии и зуда.
2. Улучшение: частичное подсушивание старых элементов, уменьшение зуда.
3. Состояние без перемен: отсутствие изменений кожных покровов.
4. Ухудшение: усиление мокнутия, появление зуда, болезненности кожных покровов.
Для оценки эффективности терапии на втором этапе лечения использовались следующие критерии.
1. Выраженное улучшение: разрешение старых элементов, отсутствие зуда и болезненности кожных покровов.
2. Улучшение: неполное разрешение старых элементов, отсутствие зуда и болезненности кожных покровов.
3. Состояние без перемен: отсутствие изменений кожных покровов.
4. Ухудшение: ухудшение клинической картины, появление зуда, болезненности кожных покровов.
Результаты и обсуждение
Пациенты за время исследования отметили хорошую эффективность и переносимость наружных препаратов: спрея, лосьона (суспензии) и крема Неотанин. Неотанин продемонстрировал выраженный противозудный эффект (рис. 4). Через 3 дня применения препарата интенсивность зуда снизилась на 37,5 % у всех пациентов, на 75 % — через неделю применения препарата. На 10-й день применения Неотанина интенсивность зуда снизилась на 80 %.
Время прекращения зуда после нанесения от 3 до 15 минут (в среднем 5 минут). Длительность противозудного действия после нанесения составила от 1 до 6 часов (в среднем 3 часа).
Неотанин достоверно снижал выраженность эритемы (гиперемии) и отечности кожных покровов (рис. 5). Регресс эритемы отмечался у 79 % пациентов на 3-й день лечения. Через неделю от начала лечения эритема уже отсутствовала у 91 % пациентов. Выраженность отека уменьшилась у 86 % пациентов на 3-й день лечения. Через неделю применения отечность отсутствовала у 92 % пациентов. Через 2 недели у 100 % пациентов отсутствовали симптомы эритемы и отечности.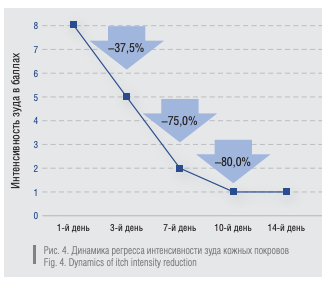
Полученные данные свидетельствуют, что препараты серии Неотанин достоверно снижали проявления воспалительной экссудации (рис. 6). Выраженное мокнутие прекратилось у 88 % пациентов на 3-й день применения Неотанина. Через неделю применения мокнутие отсутствовало у всех пациентов.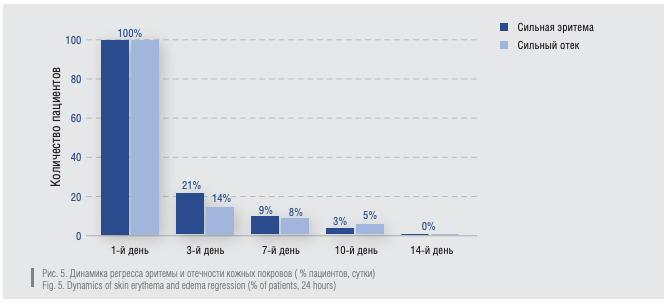
Применение препарата Неотанин достоверно уменьшало площадь поражения (воспаления кожи) (рис. 7). Площадь воспалительных изменений кожи уменьшалась через неделю на 43 % у 66 пациентов, к концу лечения — на 71 % от первоначального размера у 41 пациента, продолжавшего терапию до 5-го визита. Для оценки состояния качества жизни всех пациентов, включенных в исследование, использовали Дерматологический Индекс Качества Жизни (ДИКЖ). Данный индекс применяется дерматологами для оценки степени негативного воздействия кожного заболевания на разные аспекты жизни пациента, характеризующие качество его жизни в целом. В среднем этот показатель до лечения составил 18. К окончанию терапии он снизился до 7. Так, если до начала терапии заболевание существенно ограничивало пациентов в повседневной деятельности, то к последнему визиту абсолютное большинство больных указало на незначительное влияние состояния кожи на полноценность жизнедеятельности.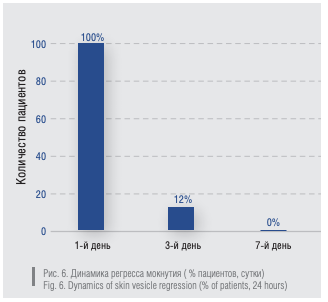
Оценка эффективности терапии Неотанином производилась по динамике уменьшения признаков экссудативного воспаления (оценка первого этапа лечения, рис. 8). У 82 % пациентов с экзематозными дерматозами наблюдалось выраженное улучшение и улучшение состояния кожных покровов, у 18 % пациентов — состояние без перемен или ухудшение.
На фоне проведенной терапии препаратами Неотанин спрей или лосьон (суспензия) и крем для наружного применения получены следующие данные по оценки эффективности терапии на втором этапе лечения (табл. 2).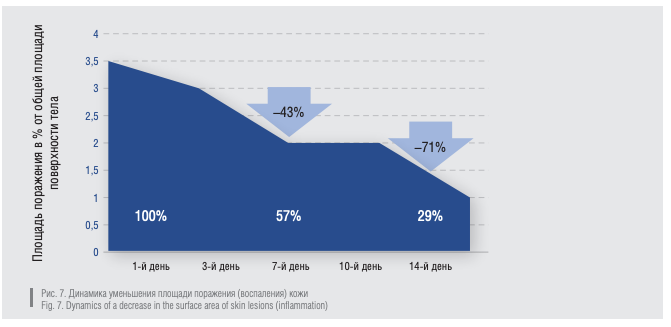
На 3-й день от начала лечения выраженное улучшение (разрешение старых элементов, отсутствие зуда и болезненности кожных покровов) отмечалось у 14,7 % пациентов, улучшение (неполное разрешение старых элементов, отсутствие зуда) — у 67,6 % пациентов. На 7-й день от начала лечения (±2 дня) выраженное улучшение отмечалось у 40,3 % пациентов, улучшение — у 41,8 % пациентов. На 10-й день от начала лечения (±2 дня) выраженное улучшение отмечалось у 35,3 % пациентов, улучшение — у 52,9 % пациентов. На 14-й день от начала лечения (±2 дня) выраженное улучшение отмечалось у 55,3 % пациентов, улучшение — у 42,1 % пациентов.
У пациентов, принимавших участие в исследовании, не было зафиксировано ни одного серьезного нежелательного явления тяжелой степени, представляющего угрозу жизни, вызвавшего постоянную или значительную утрату трудоспособности, необходимость госпитализации либо потребовавшего интенсивной неотложной терапии.
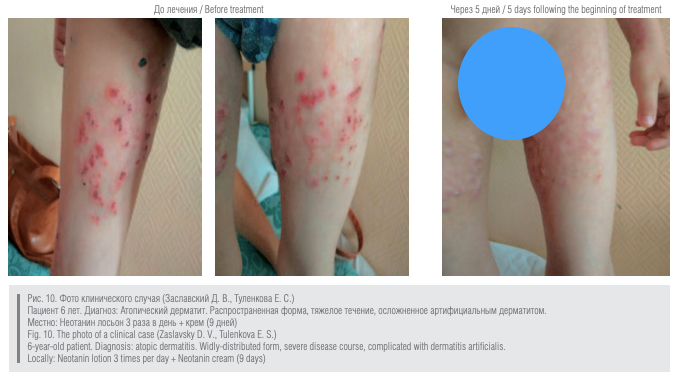
Было зарегистрировано 1 несерьезное нежелательное явление средней степени тяжести, потребовавшее отмены препарата: у пациентки с экземой кистей средней степени тяжести при первом нанесении препарата было отмечено жжение кожи, несмотря на которое, лечение было продолжено. На 10-й день лечения пациентка прекратила участие в исследовании из-за усиления жжения, зуда, отека и эритемы; после нанесения топических ГКС и приема антигистаминного препарата все симптомы купировались. У двух пациенток при переходе со спрея на крем было зарегистрировано усиление зуда и гиперемии, при возврате в терапию спрея в дополнение к крему Неотанин все симптомы купировались, пациентки завершили исследование по протоколу.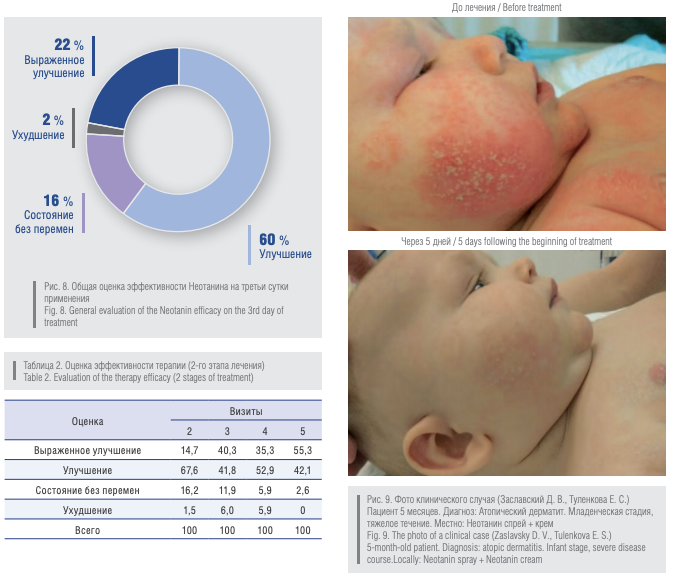
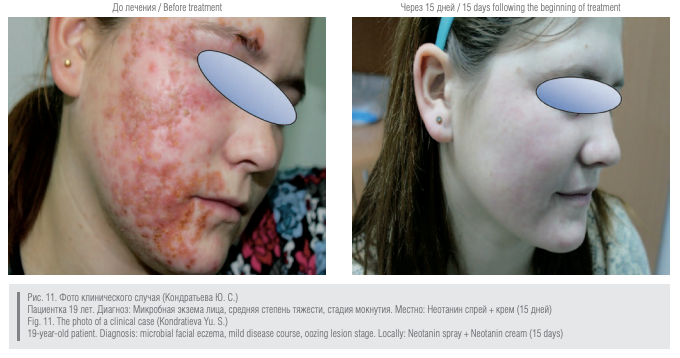
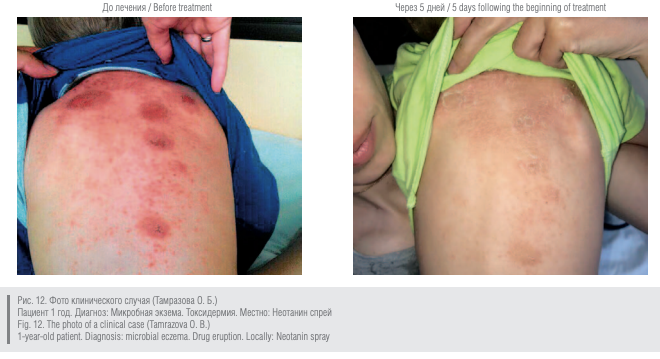
Выводы
Проведенное клиническое исследование подтверждает эффективность и безопасность спрея, лосьона (суспензии) и крема Неотанин в терапии пациентов, страдающих экзематозными дерматозами, и позволяет рекомендовать данные препараты у пациентов разных возрастов (с рождения), в том числе у беременных, с различными клиническими проявлениями заболеваний.
1. Препараты Неотанин высокоэффективны в острую и подострую стадию воспалительного процесса в качестве противозудного средства. Через неделю применения выраженность зуда уменьшилась на 75 %. Зуд купировался в течение 5 минут после нанесения препаратов, противозудный эффект длился в среднем 3–4 часа.
2. Неотанин показал выраженное регенерирующее действие, что проявлялось быстрым восстановлением целостности кожных покровов. Уже на 3-й день выраженные экскориации отсутствовали у 85 % пациентов.
3. Неотанин продемонстрировал выраженное противовоспалительное действие. Так, через неделю применения симптомы эритемы и отечности регрессировали у 92 % пациентов, достоверно уменьшились проявления воспалительной экссудации, уже через неделю мокнутие отсутствовало у 100 % пациентов.
4. Площадь поражения (воспаления) кожи уменьшилась на 71 % через 2 недели применения препарата.
5. Лекарственные формы Неотанина позволяют дифференцированно назначать его в зависимости от стадии воспалительного процесса в коже: в стадии обострения с мокнутием — спрей и лосьон (суспензия), при остром или подостром воспалении без мокнутия — крем.
6. Отсутствие серьезных нежелательных эффектов у пациентов за время наблюдения свидетельствует о хорошей переносимости и безопасности данного препарата. Заключение Таким образом, Неотанин спрей, лосьон (суспензия) и крем для наружного применения показали высокую эффективность у пациентов с экзематозными дерматозами, в том числе с мокнутием и вторичным инфицированием.
Литература/References
1. Павлов С. Т. Учебник кожных и венерических болезней. Москва: Медицина, 1969:464. [Pavlov S. T. Textbook of skin and venereal diseases. Moscow: 1969:464. (In Russ.)]
2. Самцов А. В., Барбинов В. В. Дерматовенерология. Учебник. Санкт-Петербург: Спецлит, 2008:351. [Samzov A. V., Barbinov V. V. Dermatovenereology. Textbook. Saint Petersburg, 2008:351. (In Russ.)]
3. Дарье Ж. Основы дерматологии. Москва; Ленинград: Государственное издательство: 1930:1068. [Darier J. Precis de dermatologie. Moscow; Saint Petersburg, 1930:1068. (In Russ.)]
4. Гебра Ф. Руководство к изучению болезней кожи. Санкт-Петербург: Издание О. И. Бакста: 1876:781. [Hebra F. A guide to the study of skin diseases. Saint Petersburg: The edition of O. I. Bakst: 1876:781. (In Russ.)] 5. Sulzberger M. B., Goodman J. The Relative Importance of Specific Skin Hypersensitivity in Adult Atopic Dermatitis. J.A.M.A. 1936;106:1000.
6. Malcolm M. Diseases of the Skin. An Outline of the Principles and Practice of Dermatology. London: Cassell and Company, 1903;642.
7. Sigurdsson V. et al. Expression of VCAM-1, ICAM-1, E-selectin, and P-selectin on endothelium in situ in patients with erythroderma, mycosis fungoides and atopic dermatitis. J Cutan Pathol. 2000;27(3):436–440.
8. Fierro M. T. et al. Expression pattern of chemokine receptors and chemokine release in inflammatory erythroderma and Sezary syndrome. Dermatology. 2006;213(2):284–292.
9. Calonje E., Brenn T., Lazar A., McKee P. McKee’s Pathology of the Skin, 4rd ed. Philadelphia: Elsevier-Mosby, 2011:1096.
10. Haslam E. et al. Astringency and polyphenol protein interactions. In: Romeo JT, ed. Phytochemicals in human health protection, nutrition, and plant defense. 1999:289–319.
11. Fölster-Holst, Eva Latussek. Synthetic Tannins in Dermatology — A Therapeutic Option in a Variety of Pediatric Dermatoses. Pediatric Dermatology. 2007;24(3):296–301.
12. Puschmann M., Matthies C. Synthetischer Gerbstoff im antipruriginösen und lokalanästhetischen Wirksamkeitstest. Kinderarzt. 1985;16:715–717.
13. Wiedow O. et al. The effect of tamol on humanmast cell chymase and plasmin. Skin Pharmacol. 1997;10:90–96.
14. Mrowietz U. et al. Selective inactivation of human neutrophil elastase by synthetic tannin. J Invest Dermatol. 1991;97:529–533.
15. Fölster-Holst R. Indications for tannin therapy in dermatology. European Society for Pediatric Dermatology 8th Congress. Budapest, 2005:31–32.
16. Mrowietz U., Keine P., Wiedow O. Lokaltherapie mit synthetischem Gerbstoff — Erfahrungen mit einer neuen Anwendungsform. Dt Dermatol. 1995;43:563–569.
Вам также может быть интересно