Вопросы противозудной терапии на фоне ксероза кожи
2021.10.28Л. С. Круглова, Е. В. Типаева ФГБУ ДПО «Центральная государственная медицинская академия» Управления делами Президента России, Москва ГУЗ «Саратовский областной клинический кожно-венерологический диспансер», г. Саратов
РЕЗЮМЕ
Взаимосвязь ксероза с различными кожными заболеваниями весьма многогранна, в то же время ксероз может быть причиной возникновения или усугубления зуда. Современные рекомендации по наружному лечению хронических дерматозов, сопровождающихся ксерозом и зудом, подразумевают два направления: непосредственно терапевтические мероприятия в период обострения и использование дерматокосметики, адаптированной к определенным симптомам.
Материал и методы. Под нашим наблюдением находилось 26 пациентов (средний возраст 38,7 ± 1,9 года с атопическим дерматитом, экземой, псориазом или кожным зудом, где в клинической картине присутствовал ксероз и отмечался зуд. Все пациенты использовали топические лекарственные препараты в соответствии с нозологией, в качестве адъювантной терапии – крем Неотанин Комфорт Плюс.
Результаты исследования. При атопическом дерматите показатель корнеометрии увеличился в среднем на 21%, при экземе – на 20%, при псориазе – на 22%, при кожном зуде – на 12%. Трансэпидермальная потеря воды снизилась: при атопическом дерматите – на 19,8%, при экземе – на 22,8%, при псориазе – на 21,8%, при кожном зуде – на 18,4%. Значение суммарного индекса BRS снизилось более чем в два раза.
Вывод. Применение крема Неотанин Комфорт Плюс в комбинации с лекарственной топической терапией (ГКС, многокомпонентные препараты) обладает высокой эффективностью и безопасностью у пациентов с атопическим дерматитом, экземой, псориазом или кожным зудом, что позволяет рекомендовать его для применения в широкой клинической практике.
КЛЮЧЕВЫЕ СЛОВА: ксероз, зуд, барьерная функция кожи, противозудная терапия, Неотанин Комфорт Плюс.
КОНФЛИКТ ИНТЕРЕСОВ. Авторы заявляют об отсутствии конфликта интересов.
Актуальность проблемы
Ксероз (сухость) одни из наиболее часто встречающихся симптомов применительно к кожной патологии, который может иметь вариабельные причины возникновения (наследственные, приобретенные (эндогенные, экзогенные) [1]. Ксероз может быть симптомом заболеваний кожи, соматической патологии (сахарный диабет, патология щитовидной железы и т. д.), результатом применения лекарственных препаратов (ретиноиды) или фототерапии, воздействия физических факторов (УФ-излучение), следствием инволютивных изменений.
Клинически ксероз характеризуется усиленной десквамацией, наличием микротрещин, при этом субъективно пациентов могут беспокоить ощущение дискомфорта, чувство стягивания, жжение, зуд. Описывая локальный статус, практический врач может констатировать этот симптом у большинства пациентов с кожной патологией. Взаимосвязь ксероза с различными кожными заболеваниями весьма многогранна: ксероз может быть обусловлен патогенетическими механизмами развития дерматоза (ихтиоз, атопический дерматит), может вторично возникать на фоне дерматоза (псориаз, пруриго), быть причиной развития кожного заболевания (экзема, пиодермии), являться следствием длительного медикаментозного лечения или фототерапии [2]. В большинстве этих клинических ситуаций превалирует генетическая составляющая. Так наследственно обусловленная сухость кожи объясняется генетическими мутациями, приводящими к структурным и функциональным нарушениям в поверхностных слоях эпидермиса, которые при наличии триггеров реализуются в различные аллергические заболевания. В исследованиях была выявлена группа тканевых специфических генов 1q21, 3q21, 17q25, 20p, контролирующих состояние эпидермального барьера, иммунитет и воспаление и тем самым влияющих на формирование фенотипа кожных заболеваний [3]. Еще одним хорошо изученным наследственным фактором развития ксероза является мутация гена FLG, контролирующего синтез белка филаггрина, дефицит которого приводит к повышенной трансэпидермальной потере воды и нарушению барьерной функции кожи. На сегодняшний день известно более 40 «нулевых» мутаций в гене FLG, клинически проявляющихся ксерозом [4]. Сочетание двух мутаций в гене FLG – R501x и 2282del4 является причиной развития вульгарного ихтиоза. Снижение выработки филаггрина отмечается и у большинства пациентов с атопическим дерматитом. Другими важными факторами формирования ксероза кожи являются: повышение уровня активности сериновых протеаз 5q31 и снижение активности ингибиторов протеаз serine protease inhibitor kasaltype 5 (мутации в гене SPINK5), что, например, отмечается при синдроме Нетертона, а в сочетании с гиперглобулинемией антител класса Е обусловливает высокий риск развития атопии [5].
Одним из универсальных механизмов развития ксероза является дисбаланс составляющих межклеточного матрикса – церамидов. Церамиды относятся к основному классу липидов рогового слоя; кроме них, представлены холестерин и свободные жирные кислоты.
В роговом слое пациентов с атопическим дерматитом снижено содержание церамида, а у пациентов с ламеллярным ихтиозом уменьшается количество свободных жирных кислот в роговом слое, а церамидный профиль нарушается [6].
Приобретенная сухость кожи может отмечаться практически у любого человека. К основным причинам относятся инволютивные изменения, воздействие высушивающих факторов – неправильный уход за кожей, неблагоприятное воздействие климатических условий, профессиональные и бытовые химические агенты. В то же время приобретенный ксероз кожи отмечается при ряде соматических заболеваний, в частности при онкологических заболеваниях (желудочно-кишечного тракта, болезнь Ходжкина, лимфомы), инфекционной патологии (ВИЧ/СПИД, вирусные гепатиты), психических расстройствах (психогенная анорексия), эндокринной дисфункции (заболевания щитовидной железы, сахарный диабет), почечной недостаточности, при соблюдении разных диет, гиповитаминозах, синдроме мальабсорбции и т. д. [1, 7]. Ксероз может быть симптомом кожной токсичности на фоне применения системных лекарственных препаратов (ретиноиды, противоопухолевые и многие другие), топических (ретиноиды, бензоила пероксид), а также процедур (пилинг, лазерная терапия, фототерапия) [8].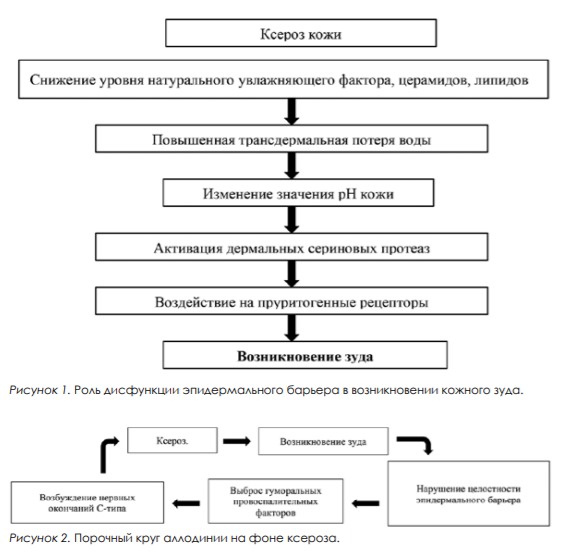
Таким образом, развитие ксероза реализуется через многочисленные механизмы, однако в конечном счете результатом является нарушение барьерной функции и повышение трансэпидермальной потери воды, что, в зависимости от генетической предрасположенности или ее отсутствии, может быть единственным клиническим симптомом или приводить к развитию или сопровождать различные кожные заболевания [8].
Кожный зуд – симптом различных заболеваний, присутствующий у более чем 50% пациентов с кожными патологиями [8, 9]. Механизмы развития зуда весьма разнообразны. Свой вклад в формирование зуда вносит и ксероз кожи (рис. 1, 2).
Современные рекомендации по наружному лечению хронических дерматозов, сопровождающихся ксерозом и зудом, подразумевают два направления: непосредственно терапевтические мероприятия в период обострения и использование дерматокосметики, адаптированной к определенным симптомам.
В настоящее время доказано, что постоянное применение увлажняющих и восстанавливающих средств является одним из основных моментов в терапии и профилактике многих заболеваний кожи [8].
На сегодняшний день арсенал топических дерматокосметических препаратов с различными механизмами действия, используемых для устранения ксероза и восстановления барьерной функции кожи, весьма обширен, что обусловливает определенные трудности в выборе наиболее оптимального средства, а значит, и необходимость дерматологам уметь ориентироваться в этом многообразии, чтобы правильно подобрать нужное средство для каждого конкретного случая [8, 9].
Материал и методы
Под нашим наблюдением находилось 26 пациентов (средний возраст 38,7 ± 1,9 года) с различными заболеваниями кожи, где в клинической картине присутствовал ксероз и отмечался зуд (см. табл.). Критерии включения в исследование: возраст 35–45 лет, фототип кожи – I, II, III по классификации Фитцпатрика, пациенты с кожным заболеванием с выраженным ксерозом и зудом, подписание информированного согласия. Критерии невключения в исследование: низкая комплаентность, участие пациента в других исследованиях, психические расстройства, хронические соматические заболевания в стадии обострения, острые воспалительные заболевания. Степень тяжести дерматозов соответствовала легкой (ограниченный процесс), что подразумевало назначение только топической терапии (см. табл.). Период наблюдения составил 4 недели. Все пациенты в качестве адъювантной терапии использовали крем Неотанин Комфорт Плюс. Активные компоненты: натуральные масла (подсолнечника, сои и карите) восстанавливают защитные функции кожи, питают кожу, делают более гладкой и эластичной; полидоканол купирует зуд; мочевина (компонент натурального увлажняющего фактора кожи) удерживает влагу в коже, предохраняет ее от пересыхания, поддерживает баланс микробиома кожи; экстракты (алоэ вера, ромашки и календулы) устраняют покраснение, раздражение, тонизируют и успокаивают кожу; витамин Е оказывает антиоксидантное действие.
За счет входящих в состав средства Неотанин Комфорт Плюс увлажняющих компонентов и противозудных активных молекул препарат позволяет решать две основные проблемы хронических заболеваний кожи – устранение зуда и восстановление барьерной функции. Оценку эффективности комбинированных методов терапии, включающих применение крема Неотанин Комфорт Плюс, проводили с учетом качественных характеристик и барьерной функции кожи, а также динамики индекса зуда через 4 недели в сравнении с показателями до терапии. Содержание воды в роговом слое эпидермиса (глубина до 100 мкм) исследовалось методом корнеометрии, которая проводилась с помощью аппарата «Скин-о-мат» (Skin-o-mat, Cosmomed, Германия). Данная методика основана на измерении электрической емкости кожи, по которой можно косвенно судить о содержании в ней воды. За основной параметр корнеометрии принимается диэлектрическая емкость самой воды, которая равна 81. Уровень ТЭПВ (трансэпидермальная потеря воды) исследовался с помощью аппарата TEWA-meter MPA 580 Courage + Khazaka (Германия). 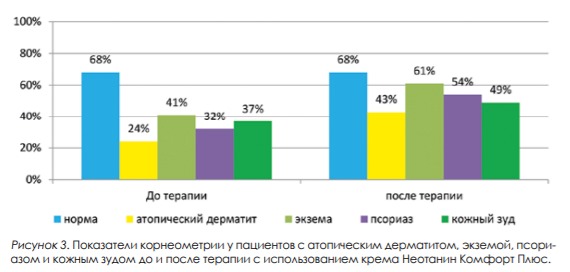
За норму принимались значения у здоровых пациентов с отсутствием кожных заболеваний в анамнезе и сопутствующей соматической патологией, влияющей на состояние кожных покровов. Нормальная, здоровая кожа, в полной мере выполняющая свою барьерную функцию, характеризуется достаточно низким уровнем ТЭПВ – до 14 г/м². В работе использовался индекс зуда Behavioral rating scores (BRS), который состоит из двух вопросов и используется для анализа выраженности зуда и вызываемого им нарушения повседневной деятельности в дневное и ночное время. Пациент отвечает на оба вопроса и полученные баллы суммируются так, что минимально возможное значение баллов – 0, а максимально возможное – 8 баллов. Статистическая обработка полученных данных проводилась с использованием статистической программы Statistica 10 с применением методов для малых выборок.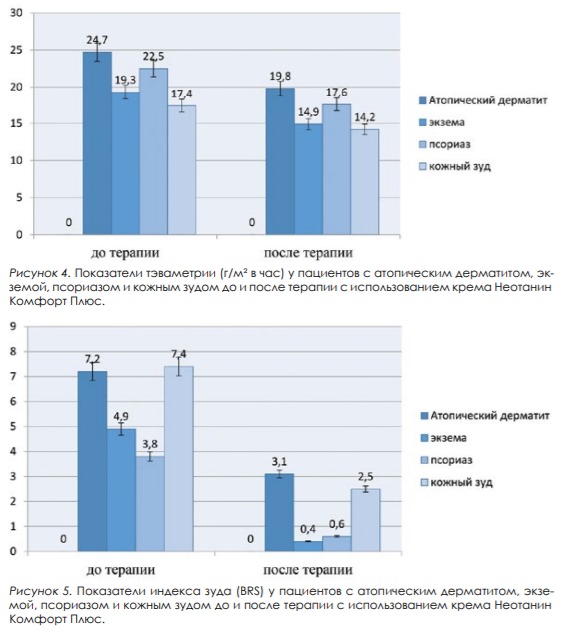
Результаты исследования
После комплексной терапии показатель корнеометрии, отражающий увлажненность кожи, улучшился у всех пациентов. При атопическом дерматите показатель увеличился в среднем на 21%, при экземе – на 20%, при псориазе – на 22%, при кожном зуде – на 12% (рис. 3). Меньшее значение при кожном зуде, по-видимому, объясняется более высокими исходными значениями показателя корнеометрии. Уровень трансэпидермальной потери воды до лечения был значительно повышен по сравнению с нормальным значением и составил от 24,7 ± 1,1 г/м² в час при атопическом дерматите (р < 0,01) до 17,4 ± 0,6 г/м² в час (р < 0,01) при кожном зуде против нормы 13,4 ± 1,0 г/м² в час. После терапии ТЭПВ снизился: при атопическом дерматите – на 19,8% (18,9 ± 1,3 г/м² в час; р = 0,0139), при экземе – на 22,8% (14,9 ± 0,7 г/м² в час; р = 0,0108), при псориазе – на 21,8% (17,6 ± 0,5 г/м² в час; р = 0,0075), при кожном зуде – на 18,4% (14,2 ± 1,3 г/м² в час; р = 0,0124) (рис. 4). До терапии у всех пациентов, включенных в исследование, отмечался зуд различной степени выраженности. Наиболее высокие значения отмечались у пациентов с кожным зудом и атопическим дерматитом. После терапии положительная динамика в отношении купирования зуда отмечалась у всех пациентов. Так, значение суммарного индекса BRS снизилось при атопическом дерматите в 2,3 раза (3,1 ± 0,7 балла; р = 0,0126), при экземе – в 12,3 раза (0,4 ± 0,1 балла; р = 0,0087); псориазе – в 6,3 раза (0,6 ± 0,2 балла; р = 0,0143); кожном зуде – в 2,9 раза (2,5 ± 0,7 балла; р = 0,0076) (рис. 5). Побочные эффекты не наблюдались ни в одном клиническом случае, переносимость крема Неотанин Комфорт Плюс была хорошей. Все пациенты дали положительную оценку органолептическим свойствам и отметили удобство применения, легкость распределения на коже, хорошую впитываемость, практически отсутствие жирного блеска и липкости.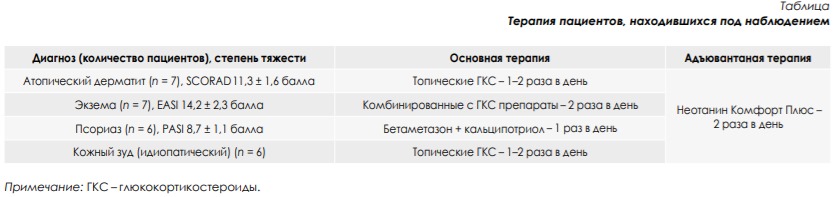
Выводы
Включение в комплексную терапию у пациентов с атопическим дерматитом, псориазом, экземой или кожным зудом топического средства Неотанин Комфорт Плюс способствует разрешению клинических симптомов дерматозов в виде восстановления кожного барьера и купирования зуда. Применение крема Неотанин Комфорт Плюс в комбинации с лекарственной топической терапией (ГКС, многокомпонентные препараты) обладает высокой эффективностью и безопасностью у пациентов с атопическим дерматитом, экземой, псориазом или кожным зудом, что позволяет рекомендовать его для применения в широкой клинической практике.
Список литературы / References
1. Тамразова О.Б. Синдром сухой кожи. Consilium Medicum. Дерматовенерология. 2014; 3: 25–31. Tamrazova O.B. Dry skin syndrome. Consilium Medicum. Dermatovenereology. 2014; 3: 25–31.
2. Тамразова О. Б., Молочков А. В. Ксероз кожи – основной патогенетический фактор развития атопического дерматита. Consilium Medicum. Дерматовенерология. 2014; 4: 48–54. Tamrazova O.B., Molochkov A.V. Skin xerosis is the main pathogenetic factor in the development of atopic dermatitis. Consilium Medicum. Dermatovenereology. 2014; 4: 48–54.
3. Cookson W. The immunogenetics of astma and eczema: a new focus on the epithelium. Nat Rev Immunol 2000; 4: 978–88.
4. Loden M, Maibach HI. Treatment of Dry Skin Syndrome. Texbook. Springer-Verlag Berlin Heidelberg. Springer, Part of Springer Science + Business Media. 2012. 3–73 р.
5. Kato A, Fukai K, Oiso N et al. Association of SPINK5 gene polymorphisms with atopic dermatitis in the Japanese population. Br J Dermatol 2003; 148: 665–9.
6. Myeong Jun Choi, Howard I. Maibach. Role of ceramides in barrier function of healthy and diseased skin. American Journal of Clinical Dermatology. 2005. Т. 6, V. 4. Р. 215–223.
7. Проценко Т.В., Проценко О.А. Синдром сухой кожи в дерматологии: механизмы формирования и лечебно-косметический уход. Украин. журн. дерматологии, венерологии, косметологии. 2009; 3: 62–5. Protsenko T.V., Protsenko O.A. Dry skin syndrome in dermatology: mechanisms of formation and medical and cosmetic care. Ukrainian Journal of Dermatology, Venereology, Cosmetology. 2009; 3: 62–5.
8. Коваленко Ю. А., Круглова Л. С., Шатохина Е. А. Современные представления о механизмах развития и фармакотерапии кожного зуда. Клиническая дерматология и венерология. 2021. Т. 20. № 1. С. 90–96. Kovalenko Yu.A., Kruglova L. S., Shatokhina E.A. Modern ideas about the mechanisms of development and pharmacotherapy of pruritus. Clinical Dermatology and Venereology. 2021. V. 20. No. 1. P. 90–96.
9. Круглова Л. С., Переверзина Н. О., Коваленко Ю. А. Противозудная терапия как основная составляющая повышения качества жизни пациентов с дерматозами. Медицинский Алфавит. 2020. 6 (420). Том 1. С. 6–11. Kruglova L. S., Pereverzina N. O., Kovalenko Yu.A. Antipruritic therapy as the main component of improving the quality of life of patients with dermatoses. Medical Alphabet. 2020. 6 (420). V. 1. P. 6–11.
Сведения об авторах
Круглова Лариса Сергеевна, д.м.н., проф., зав. кафедрой дерматовенерологии и косметологии.
ORCID: 0000–0002–5044–5265
Типаева Екатерина Владимировна, врач дерматовенеролог.
ORCID: 0000–0001–7821–4736
ФГБУ ДПО «Центральная государственная медицинская академия» Управления делами Президента России, Москва
ГУЗ «Саратовский областной клинический кожновенерологический диспансер», г. Саратов
Автор для переписки: Круглова Лариса Сергеевна. E-mail: kruglovals@mail.ru
Вам также может быть интересно